Kakexia pisu galera, gihar eta gantz ehunen atrofia eta hantura sistemikoak ezaugarritzen duen gaixotasun sistemikoa da. Kakexia minbizia duten pazienteen konplikazio eta heriotza-kausa nagusietako bat da. Kalkulatzen da kakexiaren intzidentzia minbizia duten pazienteen artean % 25etik % 70era irits daitekeela, eta mundu osoan 9 milioi pertsona inguruk pairatzen dutela kakexia urtero, eta horietatik % 80 diagnostikoaren urtebeteko epean hiltzea espero da. Gainera, kakexiak nabarmen eragiten dio pazientearen bizi-kalitateari (QOL) eta tratamenduarekin lotutako toxikotasuna areagotzen du.
Kakexiaren aurkako esku-hartze eraginkorra oso garrantzitsua da minbizia duten gaixoen bizi-kalitatea eta pronostikoa hobetzeko. Hala ere, kakexiaren mekanismo patofisiologikoen ikerketan aurrerapen batzuk egin diren arren, mekanismo posibleetan oinarrituta garatutako sendagai asko partzialki eraginkorrak edo eraginkorrak ez dira. Gaur egun, ez dago AEBetako Elikagai eta Sendagaien Administrazioak (FDA) onartutako tratamendu eraginkorrik.
Kakexia (xahutze-sindromea) oso ohikoa da minbizi mota asko dituzten pazienteengan, eta askotan pisua galtzea, gihar-xahutzea, bizi-kalitatearen murrizketa, funtzioaren narriadura eta biziraupena laburtzea eragiten du. Nazioartean adostutako estandarren arabera, sindrome multifaktorial hau gorputz-masaren indizea (GMI, pisua [kg] altuerarekin [m] karratu zatituta) 20 baino txikiagoa izatea bezala definitzen da, edo, sarkopenia duten pazienteen kasuan, sei hilabetetan % 5 baino gehiagoko pisua galtzea, edo % 2 baino gehiagoko pisua galtzea. Gaur egun, Estatu Batuetan eta Europan ez da minbiziaren kakexia tratatzeko bereziki onartutako sendagairik, eta horrek tratamendu-aukera mugatuak ditu.
Minbizi aurreratua duten pazienteen gosea eta pisua hobetzeko olanzapina dosi txikia gomendatzen duten jarraibide berriak, neurri handi batean, zentro bakarreko ikerketa baten emaitzetan oinarritzen dira. Horrez gain, progesterona analogoen edo glukokortikoideen epe laburrerako erabilerak onura mugatuak ekar ditzake, baina albo-ondorio kaltegarriak izateko arriskua dago (adibidez, progesterona erabiltzea gertakari tronboenbolikoekin lotuta). Beste sendagai batzuen entsegu klinikoek ez dute erakutsi behar adina eraginkortasunik arauzko baimena lortzeko. Anamorina (hazkunde hormona askatzen duten peptidoen ahozko bertsioa) Japonian onartu den arren minbiziaren kakexia tratatzeko, sendagaiak gorputzaren osaera neurri batean bakarrik handitu zuen, ez zuen heldulekuaren indarra hobetu, eta azkenean ez zuen AEBetako Elikagai eta Sendagaien Administrazioak (FDA) onartu. Minbiziaren kakexiarako tratamendu seguru, eraginkor eta zuzenduen premiazko beharra dago.
Hazkuntza-diferentziazio faktorea 15 (GDF-15) estresak eragindako zitokina bat da, garunaren atzeko aldean dagoen glia-eratorritako faktore neurotrofikoen familiako hartzaile alfa-antzeko proteinari (GFRAL) lotzen zaiona. GDF-15-GFRAL bidea anorexiaren eta pisuaren erregulazioaren erregulatzaile nagusi gisa identifikatu da, eta kakexiaren patogenian zeregina du. Animalia-ereduetan, GDF-15ak kakexia eragin dezake, eta GDF-15aren inhibizioak sintoma hori arindu dezake. Gainera, minbizia duten pazienteetan GDF-15 maila altuak gorputz-pisuaren eta eskeleto-muskulu-masaren gutxitzearekin, indarraren gutxitzearekin eta biziraupen-denbora laburtzearekin lotuta daude, GDF-15aren balioa helburu terapeutiko potentzial gisa azpimarratzen duena.
ponsegromab (PF-06946860) gizatiartutako monoklonal antigorputz oso selektiboa da, zirkulazioan dagoen GDF-15ari lotzeko gai dena, eta horrela GFRAL hartzailearekiko interakzioa inhibitzen duena. 1b faseko entsegu txiki ireki batean, minbiziaren kakexia eta zirkulazioan dagoen GDF-15 maila altuak zituzten 10 paziente ponsegromabekin tratatu ziren eta pisuan, gosean eta jarduera fisikoan hobekuntzak erakutsi zituzten, serumeko GDF-15 mailak inhibitzen ziren bitartean eta albo-ondorioak baxuak ziren bitartean. Horretan oinarrituta, 2. faseko entsegu kliniko bat egin genuen ponsegromaben segurtasuna eta eraginkortasuna ebaluatzeko minbiziaren kakexia eta zirkulazioan dagoen GDF-15 maila altuak zituzten pazienteetan, plazeboarekin alderatuta, GDF-15 gaixotasunaren patogenia nagusia dela dioen hipotesia probatzeko.
Ikerketan minbiziarekin lotutako kakexia (biriketako minbizia ez-zelula txikia, pankreako minbizia edo koloneko eta ondesteko minbizia) zuten helduen pazienteak sartu ziren, gutxienez 1500 pg/ml-ko GDF-15 maila serikoa, ≤3ko Ekialdeko Tumoreen Partzuergoaren (ECOG) egoera fisikoaren puntuazioa eta gutxienez 4 hilabeteko bizi-itxaropena zutenak.
Izena eman zitzaien pazienteei ausaz esleitutako 3 ponsegromab dosi (100 mg, 200 mg edo 400 mg) edo plazeboa jasotzeko, azalpean, 4 astean behin, 1:1:1 proportzioan. Amaierako helburu nagusia gorputz-pisuaren aldaketa izan zen oinarrizko mailarekin alderatuta 12 astetan. Bigarren mailako amaiera-puntu nagusia anorexia-kakexia azpieskalan (FAACT-ACS) oinarrizko mailatik izandako aldaketa izan zen, anorexia-kakexiaren funtzio terapeutikoaren ebaluazioa. Beste bigarren mailako amaiera-puntu batzuk minbiziarekin lotutako kakexia sintomen egunkariko puntuazioak, jarduera fisikoaren oinarrizko aldaketak eta osasun-gailu digital eramangarriak erabiliz neurtutako ibiltzeko amaiera-puntuazioak izan ziren. Gutxieneko erabilera-denboraren eskakizunak aldez aurretik zehazten dira. Segurtasun-ebaluazioak tratamenduan zehar izandako gertaera kaltegarrien kopurua, laborategiko proben emaitzak, bizi-zeinuak eta elektrokardiogramak barne hartu zituen. Amaierako helburu esploratorioek bizkarreko gihar eskeletikoen indizearen (gihar eskeletikoen azalera altueraren karratuz zatitua) oinarrizko aldaketak izan zituzten, gihar eskeletiko sistemikoekin lotuta.
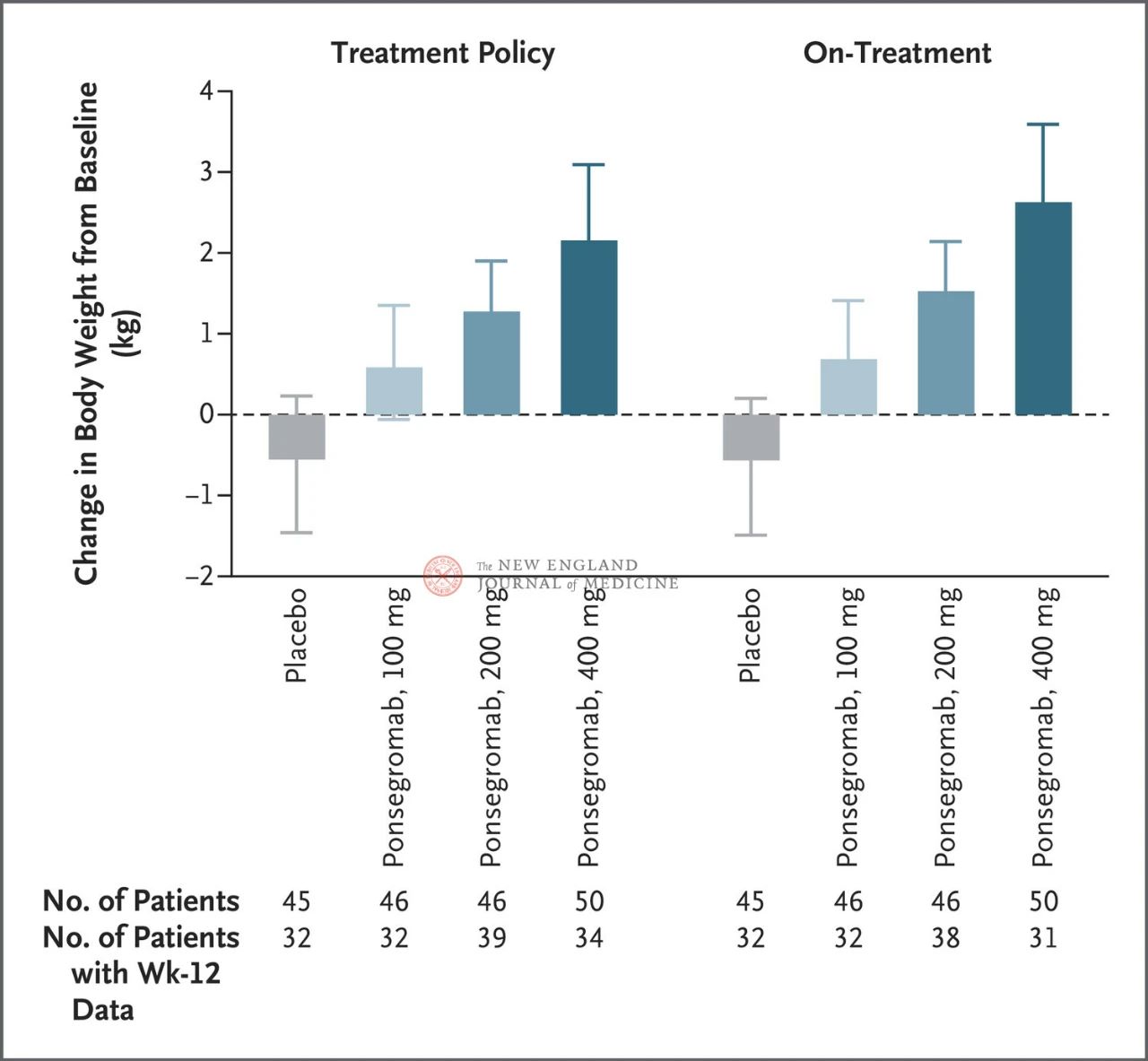
Guztira 187 paziente ausaz esleitu ziren ponsegromab 100 mg (46 paziente), 200 mg (46 paziente), 400 mg (50 paziente) edo plazeboa (45 paziente) jasotzeko. Hirurogeita hamalauk (% 40) biriketako minbizi ez-zelula txikia zuten, 59k (% 32) pankreako minbizia zuten eta 54k (% 29) ondesteko minbizia zuten.
100 mg, 200 mg eta 400 mg-ko taldeen eta plazeboaren arteko aldeak 1,22 kg, 1,92 kg eta 2,81 kg izan ziren, hurrenez hurren.
Irudiak minbizi-kakexia duten pazienteen amaiera-puntu nagusia erakusten du (oinarrizko mailatik 12 astera arteko gorputz-pisuaren aldaketa) ponsegromab eta plazebo taldeetan. Heriotza-arrisku lehiakorra eta beste gertaera bateragarri batzuk, hala nola tratamendua etetea, doitu ondoren, amaiera-puntu nagusia Emax eredu estratifikatu baten bidez aztertu zen, Bayesian joint longitudinal analisi bateko 12. asteko emaitzak erabiliz (ezkerrean). Amaiera-puntu nagusiak ere modu berean aztertu ziren, benetako tratamendurako aurreikusitako helburuak erabiliz, non gertaera bateragarri guztien ondorengo behaketak moztu ziren (eskuineko irudia). Konfiantza-tarteak (artikuluan adierazita)
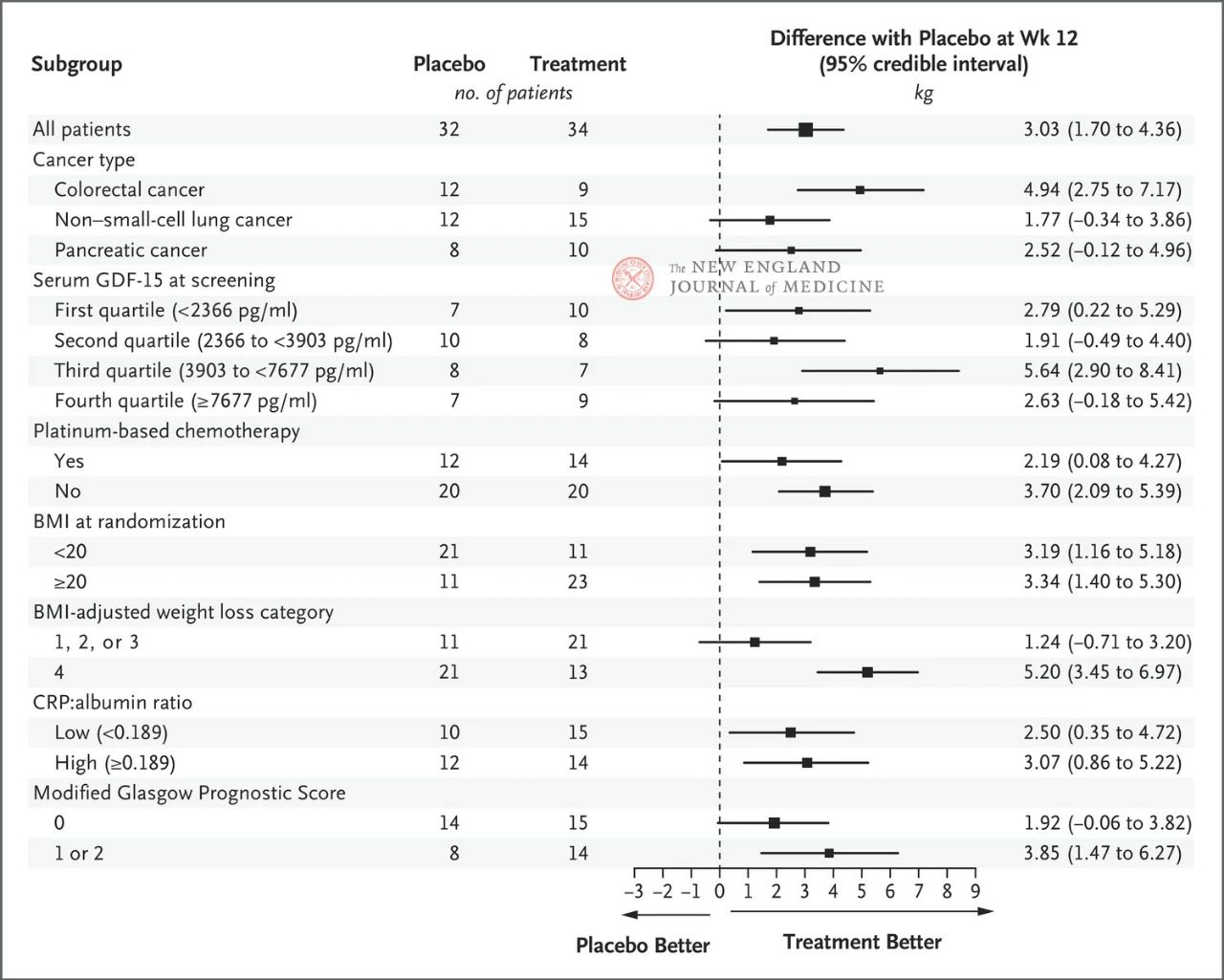
400 mg-ko ponsegromaben gorputz-pisuan izandako eragina koherentea izan zen aurretiko azpitalde nagusietan, besteak beste, minbizi mota, serumeko GDF-15 maila kuartila, platinoan oinarritutako kimioterapiaren esposizioa, GMI eta oinarrizko hantura sistemikoa. Pisuaren aldaketa koherentea izan zen GDF-15 inhibizioarekin 12 astetan.
Azpitalde nagusien hautaketa Bayes-en ondorengo analisi longitudinal bateratu batean oinarritu zen, tratamendu-estrategiaren helburu estimatuaren arabera heriotza-arrisku lehiakorra doitu ondoren egin zena. Konfiantza-tarteak ez dira erabili behar hipotesi-probak egiteko ordezko gisa doikuntza anitz egin gabe. GMIk gorputz-masaren indizea adierazten du, CRPk C proteina erreaktiboa eta GDF-15ek hazkuntza-diferentziazio faktorea 15.
Oinarrizko fasean, ponsegromab 200 mg-ko taldeko pazienteen proportzio handiagoak ez zuen gosearen jaitsierarik izan; plazeboarekin alderatuta, ponsegromab 100 mg-ko eta 400 mg-ko taldeetako pazienteek gosearen hobekuntza izan zuten oinarrizko fasetik 12 astetan, FAACT-ACS puntuazioetan 4,12 eta 4,5077ko igoerarekin, hurrenez hurren. Ez zen alde esanguratsurik egon FAACT-ACS puntuazioetan 200 mg-ko taldearen eta plazebo taldearen artean.
Aurrez zehaztutako erabilera-denboraren eskakizunak eta gailuaren arazoen ondorioz, 59 eta 68 pazientek, hurrenez hurren, oinarrizko mailarekin alderatuta jarduera fisikoaren eta ibilketaren amaierako puntuen aldaketei buruzko datuak eman zituzten. Paziente horien artean, plazebo-taldearekin alderatuta, 400 mg-ko taldeko pazienteek jarduera orokorraren igoera izan zuten 12 astetan, eguneko 72 minutuko igoera izanik jarduera fisiko ez-sedentarioarekin. Horrez gain, 400 mg-ko taldeak ere gerrialdeko gihar eskeletikoen indizearen igoera izan zuen 12. astean.
Gertakari kaltegarrien intzidentzia % 70ekoa izan zen ponsegromab taldean, plazebo taldean % 80arekin alderatuta, eta minbiziaren aurkako terapia sistemikoa aldi berean jasotzen zuten pazienteen % 90ean gertatu zen. Goragalea eta oka egitearen intzidentzia txikiagoa izan zen ponsegromab taldean.
Argitaratze data: 2024ko urriaren 5a